まとめ
◇新型コロナウイルスの収束の時期を予測してみた
①治療薬は2020年Q3(第三四半期)から利用可能となる
②ワクチンは2021年Q2(第二四半期)から利用可能となる
③上記の状況から、収束の目途がつくのは2021年Q3(第三四半期)になってからと予想します
今回のテーマは新型コロナウイルス(COVID-19)はいつ収束するかの予想です。「新型コロナウイルスの感染シミュレーション」の記事を書いたのは新型コロナウイルスとの戦いは長期戦になると懸念したからです。東京オリンピックは2020年の開催を断念し来年に延期されましたが、私は、これでもかなりリスキーだと考えています。
新型コロナウイルス(COVID-19)との戦いの鍵は、ワクチンと治療薬と思われます。先ず医薬品の開発状況を見てます。その後、感染シミュレーション結果を考慮していつ収束するかを考えてみます。
2020/04/12アップデート 治療薬とワクチンの情報を追加
2020/04/20アップデート 治療薬とワクチンの表を追加 詳しい情報はリンクを参照下さい
2020/07/28アップデート 治療薬とワクチンの情報を追加
2021/01/15アップデート 治療薬とワクチンの情報を追加
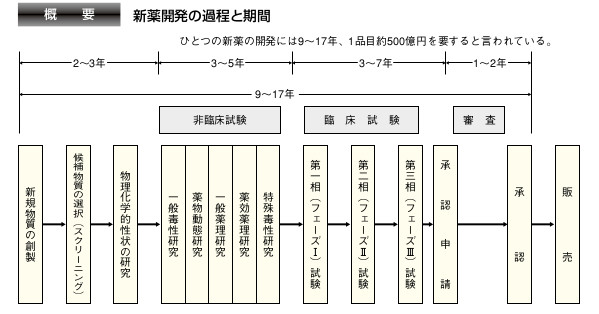
新薬開発の過程
新型コロナウイルスに対する武器は医薬品となります。新薬開発には相当の期間と開発費用が掛かるのが知られています。厚生労働省 参考1)によると1つの新薬の開発には期間:9~17年と費用:300億円が掛かるとのことです。今回は緊急を要するため、審査の迅速化と公的資金の支援が期待できます。
特に重要な臨床試験は3段階で行われます。 通常では、臨床試験には3~7年も掛かります。まず、フェーズIでは、少人数の健康な人に新薬を投与して、安全性を中心に調べる。フェーズIIでは、少人数の患者に投与して、効き目や副作用を確認するとともに最適な使い方を決める。最終フェーズIIIでは、多数の患者に投与して、効果と安全性について確認する。
治療薬
治療薬は新型コロナウイルスに感染した人に使う医薬品です。新型コロナウイルスに感染した人の死亡率は、1%程度 参考2)と従来のインフルエンザの約10倍となっています。現時点では新型コロナウイルス用に開発された治療薬は承認されていませんが、重症患者に対して治療薬を使うことが出来れば死亡率が劇的に下がることが期待されます。ただし、医療体制が維持され重傷患者が適切な治療を受けられるのが前提条件となります。
治療薬には、既存薬の転用と新規開発があります。既存薬は他の目的で既に使われている/準備されたので、前半の過程をスキップして臨床試験から開始できる時間的なメリットがあります。緊急時なので既存薬の転用に焦点を当てます。参考3)によるとQ2中を目指して、レムデシビル:ギリアド・サイエンシズ(米)、アビガン※:富士フイルム富山化学、また、Q3中を目指して、UC-MSCs:ZhiYong Peng(中国)、Tuohua Biological Technology(中国)、Huaier Granule:Tongji Hospital(中国)が開発中です。なお、抗HIV薬「カレトラ」、標準治療との比較で有効性は示されず 参考4)との判断が示されたとのことです。
※アビガンを開発された白木公康氏の寄稿 参考8)も参考になります
2020年7月28日時点では、「レムデシビル」と「デキサメタゾン」が承認されていますが、どちらも劇的な効果を示すものではないと理解しています。2021年01月07日、英国で「アクテムラ」が重症患者の治療に有効との発表がありました。また、忽那賢志 感染症専門医の記事をご参考にして頂ければ、新型コロナ患者の症状や治療法についての最新情報が得られ参考になります。
| 薬品名 | 開発・製造 | 内容とリンク |
| 血漿(けっしょう) | カナダ研究グループ他 | ・回復期患者の血漿(抗体)を治療薬として使用 |
| レムデシビル 5月07日特例承認 | ギリアド・サイエンシズ社 | ・重症患者用 ・5日間の治療に必要な分量は約25万円 |
| オルベスコ | 帝人ファーマ他 | ・喘息治療薬 ・肺炎患者 |
| アビガン 承認遅れ発生 | 富士フイルム富山化学 | ・軽症と中等症の患者他 ・インフルエンザの3倍投与 →患者当たり8,000円? |
| ヒドロキシクロロキン | ノバルティス他 | ・抗マラリア薬 |
| イベルメクチン | オーストラリアのビクトリア感染研究所 | 大村智氏(ノーベル賞受賞)が土壌の微生物から分離したアベルメクチン |
| デキサメタゾン 7月10日承認 | 既存のステロイド薬 | 厚生労働省 新型コロナウイルス感染症診療の手引き第2.2版 P29 |
| アクテムラ 英国で承認 | 中外製薬株式会社 トシリズマブ(アクテムラ) サノフィ株式会社 サリルマブ(ケブザラ) | ・大阪大学と中外製薬により共同開発されたリウマチ薬 ・ジョンソン英国首相の記者会見 |
ワクチン
新型コロナウイルスに感染しない免疫をつくるワクチンに大きな期待がかかります。治療薬と異なり、(既存薬扱いではないので)ワクチンの開発には時間が掛かりそうです。早くとも来年になる見込みです。ジョンソン・エンド・ジョンソンが具体的な開発スケジュールをアナウンス 参考5)しました。それによると今年の9月までにフェーズI治験を始める、2021年初頭に緊急用に利用可能となると見込んでいる。ファイザーとBioNTechはワクチンの開発状況を公表(4月09日)参考7)した。それによると2020年4月に人に対しての試験、2020年末までに百万オーダーのワクチン供給を目指している。他社からも、2021年のQ2〜Q3には新しいワクチン 参考3)が出てくる可能性があります。ただし、ワクチンには、抗体依存性感染増強(ADE)という問題が起きるリスク 参考6)があるとのことで慎重な治験が必要です。
2020年07月の時点でワクチンの開発はワークスピードで進んでいますが、懐疑的な見かたをする専門家(①本庶佑京都大学特別教授、②フォンタネ 仏疫学者他)も多数います。一重らせんのRNA(新型コロナウイルス)はその構造が不安定で、遺伝子が変異しやすい①、100%有効なワクチンが2021年中に開発される可能性はほとんどない②などが例です。
「2021年01月15日時点のアップデート」
ワクチンの開発は、世界で約200社がしのぎを削っているとのこと。米・EUメーカの3グループが先行し、2020年の年末には、ワクチンの供給を開始しています。日本政府は、ワクチン開発の先頭グループの欧米薬品メーカー:ファイザー、アストラゼネカ、モデルナから供給を受ける 参考9)計画です。接種開始の時期は2月下旬目標です。日本メーカーは政府のサポート不足などで周回遅れとなっています。
| 開発・製造 | 計画とリンク |
| ファイザーとBioNTech 2020/12 EU、米国他で承認 | ・2020年4月に人に対してのmRNAワクチン試験 ・2020年末までに百万オーダーのワクチン供給 |
| ジョンソン・エンド・ジョンソン(J&J) | ・臨床試験を9月までに開始 ・2021年初めの緊急的使用 |
| メディカゴ(田辺三菱製薬の子会社) | ・人での臨床試験を2020年8月までに開始 |
| モデルナ 2021/01 米国他で承認 | ・mRNAワクチンが臨床試験開始 |
| アンジェス 製造:タカラバイオ | ・DNAワクチン ・6カ月以内(2020年10月)のできる限り早い時期の臨床試験開始 |
| アストラゼネカ/オックスフォード大 2020/12 英国承認 | ・ウイルスベクターワクチン |
収束時期
現在は、人の移動を制限しかつ接触の機会も減らして、新型コロナウイルスの新たな感染者を力づくで抑えようとしている状況です。都市封鎖などの強い規制でどうにか医療体制を崩壊させない均衡点を見つけたとしても、規制を緩めた途端に感染者がまた増加し始めます。新型コロナウイルスの収束が見えてくるのは免疫を持つ人が人口の60%を超えたあたりからです。これは単純な確率論の問題で説明されます。免疫を持つ人の割合(γとする)が増えると、感染する人の数が(1-γ)に比例して減るからです。
先に述べた新型コロナウイルスの医薬品の開発状況から、最速の場合で、①感染した人に対する治療薬は2020年Q3(第三四半期=9~12月)から、②免疫をつくるワクチンは2021年Q2(第二四半期=4~6月)から、利用できると期待されます。しかし、医療体制を崩壊させないためには、徐々に緩和することは出来ますが、人の移動の制限と接触の機会の低減は引き続き継続が必要です。以上から、新型コロナウイルスの感染は2021年の年央には収束時期が見えては来るが、2021年いっぱいは混乱が続くと思われます。
参考資料
参考1)
https://www.mhlw.go.jp/za/0825/c05/pdf/21010235.pdf
参考2)
https://headlines.yahoo.co.jp/hl?a=20200331-35151613-cnn-int
参考3)
https://project.nikkeibp.co.jp/behealth/atcl/feature/00004/032500169/?P=2
参考4)
http://www.qlifepro.com/news/20200326/lopinavir-ritonavir.html
参考6)
https://bio.nikkeibp.co.jp/atcl/news/p1/20/03/30/06749/
参考8)
https://www.jmedj.co.jp/journal/paper/detail.php?id=14305
